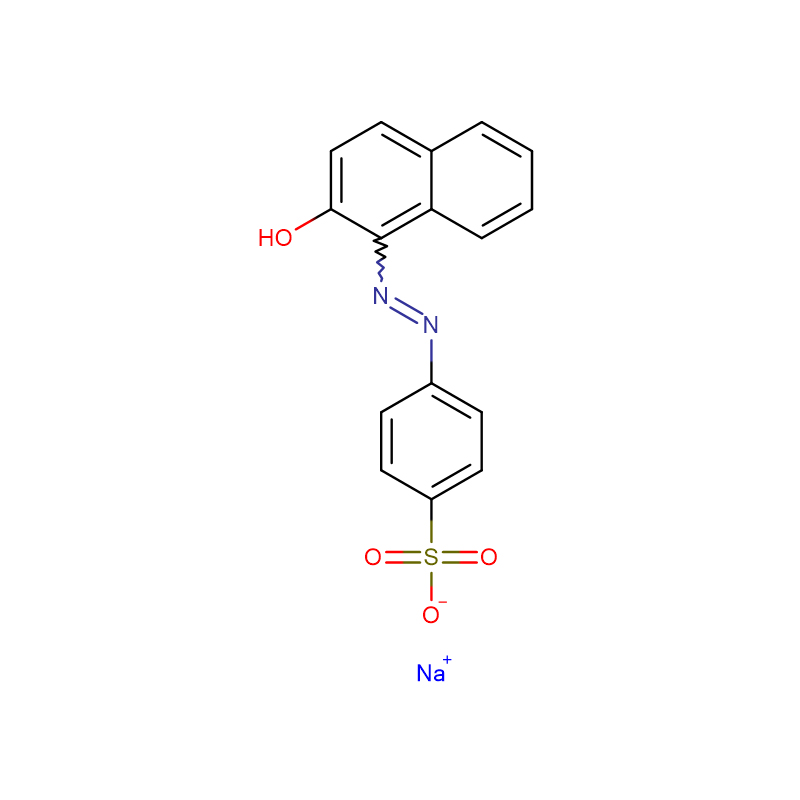
Sal de sodio naranja II CAS: 633-96-5 polvo amarillo
| Numero de catalogo | XD90466 |
| nombre del producto | Sal de sodio de naranja II |
| CAS | 633-96-5 |
| Fórmula molecular | C16H11N2NaO4S |
| Peso molecular | 350.324 |
| Detalles de almacenamiento | 2 a 8 °C |
| Código Arancelario Armonizado | 3204120000 |
Especificaciones del producto
| Punto de fusion | 164 °C |
| Apariencia | polvo amarillo |
| Ensayo | 99% |
El efecto de Cl(-) en la degradación oxidativa de Acid Orange 7 (AO7) se investigó en el sistema UV/S2O8(2-) para dilucidar las vías de cloración en aguas residuales salinas.Una menor cantidad de Cl(-) así como de Br(-) mejoró la decoloración de AO7, pero dicho efecto de promoción se redujo gradualmente con el aumento de la dosis de iones de haluro.Se encontró que la mineralización del colorante es inhibida por Cl(-), especialmente en condiciones ácidas.Los resultados del modelo cinético demostraron que la fracción de diferentes radicales oxidantes dependía en gran medida del contenido de Cl(-).Al pH inicial de 6,5, el Cl2(-) era mucho más abundante que el SO4(-).La importancia de Cl2(-) para la degradación de AO7 aumentó con el aumento de la concentración de Cl(-) y superó a la de SO4(-) a [Cl(-)]>1 mM.Sin Cl(-), SO4(-) fue el radical predominante para la degradación de AO7 en condiciones ácidas, mientras que OH prevaleció gradualmente a pH más alto.En condiciones de alta salinidad, se puede formar más OH y contribuir a la degradación del tinte, especialmente en medios alcalinos, lo que conduce a una mayor eficiencia de destrucción de AO7.Se detectaron varios subproductos clorados en presencia de iones de cloruro, y se propusieron vías de degradación de AO7 basadas en SO4(-)/Cl2(-).Este trabajo proporciona una mayor comprensión de los complejos mecanismos de reacción de los procesos de oxidación avanzada basados en SO4(-) en entornos ricos en cloruro.