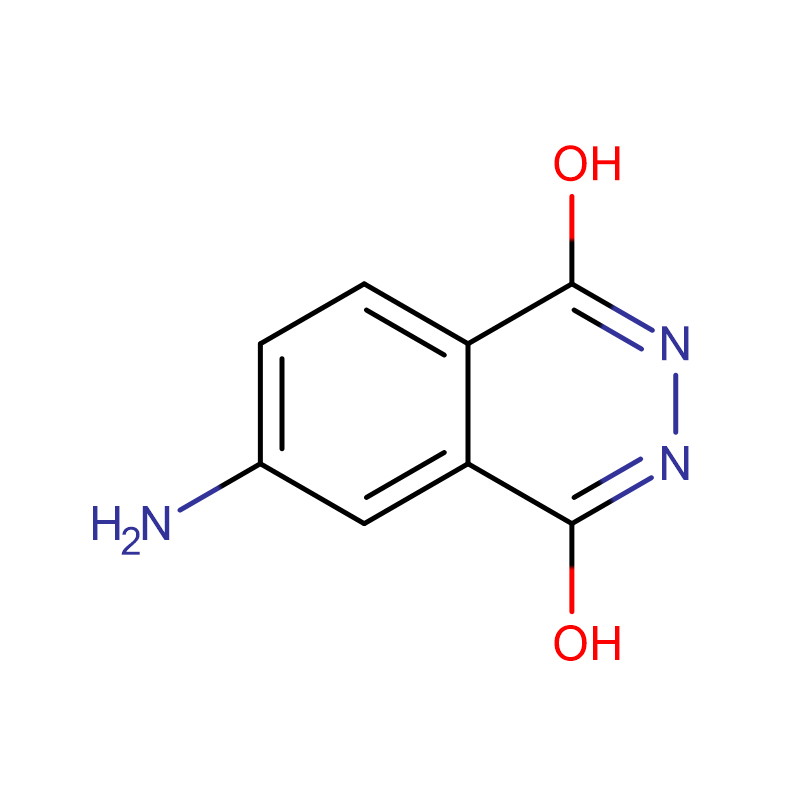
4-Aminoftalhidrazida AMPPD Cas:3682-14-2 Polvo de amarillo claro a ámbar a verde oscuro a grumos
| Numero de catalogo | XD90156 |
| nombre del producto | 4-aminoftalhidrazida |
| CAS | 3682-14-2 |
| Fórmula molecular | C8H7N3O2 |
| Peso molecular | 177.16 |
| Detalles de almacenamiento | Tienda en RT |
Especificaciones del producto
| Apariencia | Amarillo claro a ámbar a polvo verde oscuro a grumos |
| Asay | ≥98,0% |
| Densidad | 1.433 |
| Punto de fusion | 300ºC |
| Punto de ebullición | 633°C a 760 mmHg |
| punto de inflamabilidad | 336,7°C |
| Solubilidad | Soluble en hidróxido de amonio, carbonato de sodio u otra base. |
1. Analizamos y comparamos el efecto de cinco antihistamínicos H1 sobre el estallido oxidativo estimulado a nivel extracelular e intracelular de leucocitos polimorfonucleares humanos aislados y estimulados. Se estudió el estallido oxidativo de neutrófilos humanos aislados por medio de quimioluminiscencia mejorada con luminol e isoluminol. Lo siguiente El orden de potencia de los antihistamínicos H1 para disminuir la quimioluminiscencia se evaluó extracelularmente: ditiaden> loratadina> clorfeniramina> bromfeniramina> feniramina y en el sitio intracelular: loratadina> ditiaden. Los antihistamínicos H1 difieren sustancialmente según su estructura química en la supresión del estallido oxidativo tanto en extra - y sitio intracelular de neutrófilos humanos estimulados aislados.
2. Los sistemas de quimioluminiscencia mejorados con isoluminol o luminol en combinación con una peroxidasa son métodos sensibles para la detección de especies reactivas de oxígeno (ROS) generadas por la NADPH oxidasa del fagocito.Los dos sustratos amplificadores son estructuralmente muy similares y solo difieren en la posición del grupo amino en el anillo aromático de las moléculas.Esta diferencia hace que el isoluminol sea una molécula menos lipófila y menos permeable a las membranas biológicas.En consecuencia, el uso de isoluminol se restringe a estudios relacionados con la secreción de metabolitos de oxígeno.En este estudio mostramos que los péptidos sintéticos derivados del dominio N-terminal de la proteína anexina AI regulada por calcio interfieren con la detección de radicales en un sistema amplificado con isoluminol, pero no en un sistema amplificado con luminol.Los péptidos derivados de la anexina AI reducen la producción de luz con isoluminol excitado por superóxido y peroxidasa de rábano picante (HRP) en células estimuladas con formil-metionil-leucil-fenilalanina y forbol miristato acetato, así como por peróxido de hidrógeno y HRP.El mecanismo preciso para la inhibición no se conoce.Los resultados presentados sugieren fuertemente que una respuesta celular reducida detectada con quimioluminiscencia amplificada con isoluminol debe confirmarse con una técnica alternativa para determinar la liberación de aniones superóxido y peróxido de hidrógeno.